مرض وعائي غامض.. اكتشاف سبب خلل التنسج العضلي الليفي
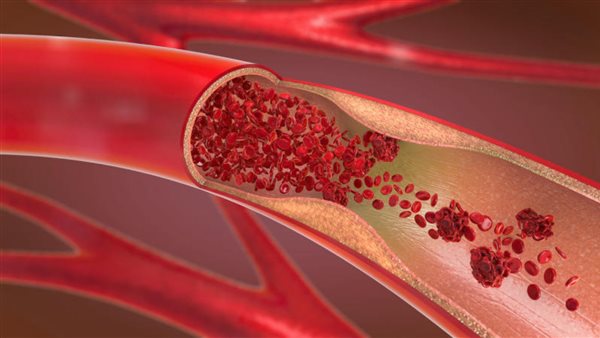
تمكن باحثون من تحديد العامل الرئيسي وراء اضطراب الأوعية الدموية المعروف باسم خلل التنسج العضلي الليفي (FMD) والذي يصيب ما يصل إلى 5% من السكان البالغين.
يمكن أن يؤدي هذا الاضطراب إلى ارتفاع ضغط الدم أو النوبة القلبية أو السكتة الدماغية.
وفي دراسة نشرت في مجلة Nature Cardiovascular Research، قال الفريق إن التغيرات في الجين UBR4 لعبت دورًا مهمًا كمحرك رئيسي لمرض FMD.
وبحسب ما نشره موقع ميديكال إكسبريس، اقترح أن هذا الاكتشاف قد يكون خطوة مهمة نحو تطوير نهج علاجي لهذا الاضطراب.
خلل التنسج العضلي الليفي
يقول جيسون كوفاسيك، أستاذ أمراض القلب، والمؤلف الرئيسي للدراسة: "على الرغم من أن خلل التنسج العضلي الليفي تم التعرف عليه لأول مرة منذ أكثر من 80 عامًا، إلا أنه حتى الآن لم يكن معروفًا سوى القليل جدًا عن أسبابه وعلم الأمراض أو علاجه المحتمل".
وأضاف: "من خلال إنشاء أول نموذج للفأر، حصلنا على رؤى حاسمة في العمليات التي تؤدي إلى الإصابة بمرض FMD، بما في ذلك دور جين ترميز البروتين UBR4 وشبكة التعبير الجيني المرتبطة به والتي تنظم وظيفة الأوعية الدموية في الجسم".
تتضمن خلل التنسج العضلي الليفي نموًا غير طبيعي للخلايا في جدران الشرايين، بما في ذلك الشرايين السباتية والكلوية والتاجية.
وعلى الرغم من إمكانية إصابة أي شخص بهذه الحالة، إلا أنها تتميز بتحيز جنسي واضح، حيث تؤثر على النساء في حوالي 90% من الحالات.
وعلى عكس أمراض الأوعية الدموية الأخرى مثل تصلب الشرايين، لا يحدث خلل التنسج العضلي الليفي بسبب تراكم اللويحات، ولا يدرك العديد من الأشخاص أنهم مصابون بهذا الاضطراب.
من بين الحالات الطبية الخطيرة التي يمكن أن تؤدي إليها - اعتمادًا على الشريان المصاب - تمدد الأوعية الدموية (انتفاخ وإضعاف الشريان)، والتشريح (تمزق جدار الشريان)، والسكتة الدماغية، والنوبة القلبية. يمكن أن يؤدي تدفق الدم المحدود من FMD أيضًا إلى ارتفاع ضغط الدم، والطنين النابض (صوت صفير في الأذنين يحدث مع كل نبضة قلب)، والصداع النصفي.
وباستخدام الأساليب الإحصائية المتقدمة المعروفة باسم "علم الأحياء النظمي"، تمكن العلماء من إنشاء أول نماذج الفئران على الإطلاق والتي تلخص جوانب معينة من المرض لدى البشر، وكشف رؤى مهمة حول مساراته السببية ومحركاته.
وقال المؤلف المشارك، جيفري دبليو أولين: "تضمنت هذه الرؤى اكتشاف أن التغيرات في مستويات UBR4 - والتي تسبب تغييرات كبيرة في مستويات التعبير عن الجينات الأخرى في الشبكة الفائقة المرتبطة بـ FMD - أدت بشكل جماعي إلى تغييرات كبيرة في وظيفة الخلايا الوعائية".
وأضاف: «أدت هذه التغييرات بدورها إلى اتساع واضح في الشرايين لدى الفئران، وهو أحد سمات داء الحمى القلاعية لدى البشر".
من خلال تحديد الجين وشبكته التنظيمية الجينية التي يبدو أنها مسؤولة عن جزء كبير من وراثة داء الحمى القلاعية، يعتقد العلماء أنهم اتخذوا خطوة كبيرة نحو الحل العلاجي.
ويؤكد الدكتور كوفاسيتش: "إن دراستنا تفتح الباب أمام التعديل المستهدف لجين UBR4 وشبكته التنظيمية الجينية المرتبطة بالمرض، وهو ما قد يحمل وعدًا هائلًا للعديد من الأشخاص، وخاصة النساء، الذين يعانون من هذه الحالة".
وأضاف: "إن هذه النتائج المثيرة تشجعنا على مواصلة عملنا مع زملائنا في جميع أنحاء العالم لإلقاء المزيد من الضوء على مرض كان حتى الآن مجرد صفحة فارغة إلى حد كبير".



