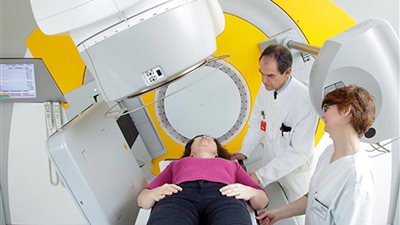
علاجات جزيئية مبتكرة تعطل نمو الخلايا السرطانية.. كيف هذا؟
تمثل دراستان جديدتان خطوة كبيرة نحو تطوير علاجات جزيئية مبتكرة قادرة على تعطيل النمو غير القابل للسيطرة للسرطانات من جذورها.
في زوج من الأوراق البحثية المنشورة مؤخرًا في مجلة Nature، أظهر فريق من العلماء بقيادة قسم الكيمياء والبيولوجيا الكيميائية في جامعة هارفارد كيف يمكن للجزيئات الصغيرة والطفرات الجينية أن تغير نفس التفاعلات البروتينية الحرجة في الخلايا السرطانية.
تقدم هذه الدراسات رؤى ثاقبة في مجالين: اكتشاف "غراء جزيئي" جديد وفهم تأثير الطفرات الجينية داخل الخلايا السرطانية، مما يمهد الطريق للأساليب العلاجية.
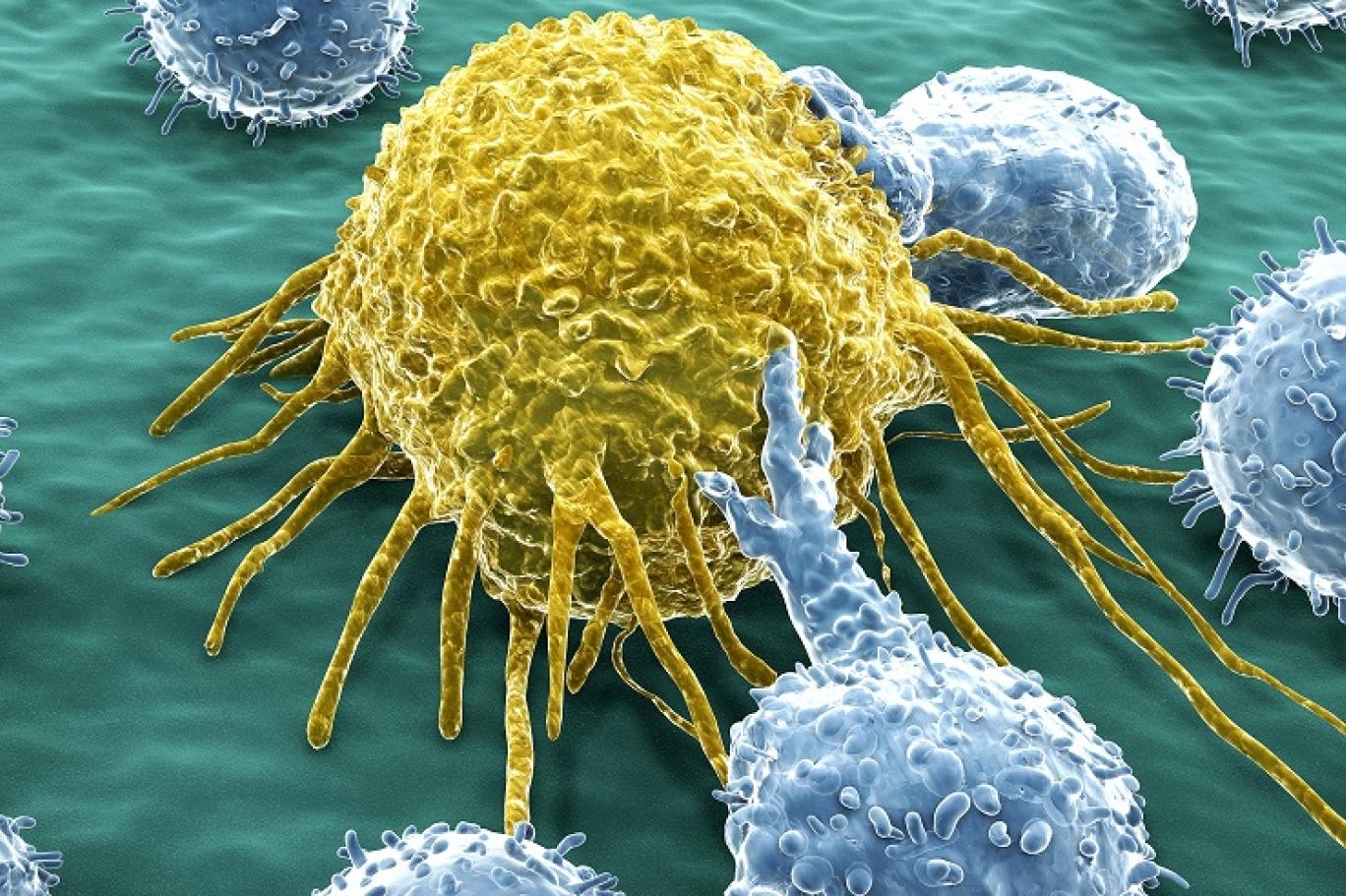
محاكاة طفرات الورم الأرومي النخاعي
قال المؤلف الرئيسي براين لياو، الأستاذ المساعد في الكيمياء والبيولوجيا الكيميائية: " ركز بحثنا على فهم كيفية محاكاة الطفرات المحددة في الورم الأرومي النخاعي، وهو سرطان يصيب المخ عند الأطفال، لعمل (الغراء الجزيئي) لدفع العمليات المسببة للسرطان".
وأوضح أنه "خلال مسار هذه الدراسات، قمنا بتفصيل التقارب بين الطفرات الجينية والوسائل الكيميائية التي تغير تفاعلات البروتين".
إن المواد اللاصقة الجزيئية عبارة عن جزيئات صغيرة تجبر بروتينين لا يتفاعلان عادة على الارتباط ببعضهما البعض، وهذا يحفز "نظام التخلص من القمامة" الطبيعي في الخلية على تحلل أحد البروتينين. وقد استكشف الباحثون إمكانية استخدام المواد اللاصقة الجزيئية لاستهداف البروتينات المسببة للأمراض.
حتى الآن، لم يتم استغلال العديد من هذه التفاعلات بسبب تعقيدها وصعوبة اكتشافها.
ومع ذلك، يكشف هذا البحث عن هيكل جديد وآلية جديدة يمكن استخدامها لتصميم مواد لاصقة جزيئية للتأثير على تفاعلات ووظائف بروتينية محددة.
وقد استكشفت إحدى الدراسات كيف تعمل المواد اللاصقة الجزيئية على تغيير شبكات التفاعل البروتيني الأساسية.
وأظهر الباحثون أن الجزيء UM171 يعمل كغراء يمكنه تحفيز تحلل مركب CoREST، وهو نظام تنظيمي يتحكم في الوصول إلى الجينات.
تعمل UM171 عن طريق التفاعل مع بروتين يسمى هيستون دياسيتيل (HDAC)، وهو جزء من مركب أكبر مع CoREST، ولصقه ببروتين آخر يسمى KBTBD4، وهو إنزيم فعال في تحلل البروتين.
تظهر هذه النتائج طرقًا جديدة لاستخدام المواد اللاصقة لاستهداف البروتينات التي كانت تعتبر تقليديًا غير قابلة للعلاج، مثل CoREST، مما يوفر استراتيجيات جديدة لتصميم الأدوية.
وقالت أوليفيا تشانج: أحد قادة العمل: "كانت كيفية عمل هذا الجزيء الصغير بمثابة سؤال كبير في هذا المجال لأنه في ذلك الوقت لم يكن أحد يعرف على وجه اليقين أنه عبارة عن غراء جزيئي، وقد توصلنا إلى هذه المشكلة من خلال نهج متعدد التخصصات، مستفيدين من كل من علم الجينوم الوظيفي وعلم الأحياء البنيوي لتزويدنا برؤى جديدة".
وفي الدراسة المرافقة، قام الباحثون بالتحقيق في الطفرات المسببة للسرطان في بروتين KBTBD4، والذي غالبًا ما يتحور في نوع من سرطان المخ.
يمكن لهذه الطفرات أن تحول التفاعلات الخلوية الطبيعية إلى تفاعلات ضارة عن طريق تغيير كيفية ارتباط البروتينات، مما يتسبب في تدهور غير طبيعي لمركب CoREST.
تمكن الفريق من تحديد الطفرات في KBTBD4 التي تساهم في الإصابة بالسرطان، ثم استخدموا المجهر الإلكتروني المبرد "لرؤية" هذه الطفرات على المستوى الذري.
بدمج هذه التقنيات، اكتشف الفريق أن الطفرات السرطانية تغير بنية البروتين ووظيفته، مما يعكس تفاعل UM171 وKBTBD4.
كانت الميزة المميزة لهذا البحث هي التركيز على "التقارب"، حيث تحاكي الجزيئة الصغيرة والطفرة الجينية بدقة تأثيرات بعضها البعض وظيفيًا وبنيويًا.
وفي مختبر لياو، استكشف الباحثون كيف يمكن لفهم آلية واحدة أن يساعد في تطوير وتطبيق آلية أخرى.
قال لياو: "من الصعب حقًا العثور على هذه الأنواع من جزيئات الغراء الجزيئية، لذا إذا كان بإمكانك بالفعل استخدام علم الوراثة للبحث عنها، فسيكون ذلك مفيدًا للغاية، فهذا التقارب الكيميائي الجيني هو نموذج جديد".
وفي المستقبل، يخطط مختبر لياو لمزيد من استكشاف هذه الاستراتيجيات الجزيئية، والبحث عن المزيد من حالات الطفرات الجينية التي يمكن أن تحفز تفاعلات بروتينية جديدة للمساعدة في التصميم الكيميائي.
وتقدم آثار هذا البحث استراتيجية جديدة لفهم البروتينات واستهدافها لاكتشاف الأدوية الجزيئية الصغيرة.