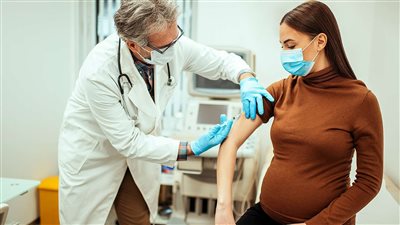
مساعٍ جديدة لتطوير لقاحات الفيروس المخلوي التنفسي
في أغلب الناس، تتسبب مسببات الأمراض التي تصيب الرئة والمعروفة باسم الفيروس المخلوي التنفسي (RSV) والفيروس الرئوي البشري (hMPV) في ظهور أعراض خفيفة تشبه أعراض البرد.
لكن في الرضع وكبار السن، يمكن أن تسبب هذه الفيروسات التهابًا رئويًا حادًا وحتى الموت.
ومع ذلك، كان من الصعب تصميم لقاحات ضد كلا الفيروسين.
الآن، قام علماء Scripps Research بتحليل بنية واستقرار بروتين مهم لفيروس المخلوي التنفسي وفيروس الجهاز التنفسي البشري لتصميم لقاحات تستهدفه بشكل أفضل.
شير بحثهم، الذي نُشر في Nature Communications، إلى لقاحات RSV التي قد تكون أكثر فعالية من اللقاحات الحالية، بالإضافة إلى لقاح ضد فيروس المخلوي التنفسي البشري، والذي لا توجد خيارات متاحة تجاريًا له.
وبحسب موقع ميديكال إكسبريس، يقول الدكتور جيانج تشو، كبير مؤلفي الدراسة: "إن ابتكار لقاح مركب لهذه الفيروسات قد يقلل بشكل كبير من حالات دخول المستشفيات بسبب الفيروس لكل من الأطفال وكبار السن، وقد يخفف هذا العبء الصحي العام خلال موسم الإنفلونزا، وهو أيضًا الوقت الذي تحدث فيه معظم حالات الإصابة بفيروس المخلوي التنفسي وفيروس الجهاز التنفسي البشري".
حاول العلماء منذ فترة طويلة ابتكار لقاحات تحفز الجهاز المناعي على التعرف على بروتينات الاندماج (F) الموجودة على أسطح فيروس المخلوي التنفسي وفيروس الإنفلونزا البشري والفيروسات ذات الصلة.
تلعب هذه البروتينات دورًا رئيسيًا في السماح للفيروسات بإصابة الخلايا البشرية.
ومع ذلك، فإن بروتين F له بنية دقيقة تتغير بسرعة من شكل "ما قبل الاندماج" إلى شكل "ما بعد الاندماج" عندما تندمج الفيروسات مع الخلايا. من الناحية المثالية، من شأن اللقاح أن يعلم الجهاز المناعي التعرف على بروتين F المغلق قبل الاندماج حتى يتمكن من إيقاف العدوى.
يقول تشو: "المشكلة هي أن هذا الهيكل قبل الاندماج هش للغاية ومتقلب، فإذا غيرت البيئة حتى ولو قليلًا، فإن البروتين يصبح أشبه بالمحول الذي يتحول فجأة من سيارة إلى روبوت".
هذا يعني أن العلماء لا يستطيعون ببساطة استخدام بروتين F المعزول قبل الاندماج كلقاح ــ إذ إن بنيته سوف تتغير بسرعة كبيرة بحيث لا يتمكن الجهاز المناعي من الاستجابة لها، ولن يدرّب اللقاح الذي يستهدف النسخة التي تلت الاندماج من البروتين الجهاز المناعي على مهاجمة الفيروس قبل أن تتاح له الفرصة لإصابة الجسم.
يعتقد تشو، الذي قام مؤخرًا بتصميم لقاحات جديدة للفيروسات بما في ذلك فيروس نقص المناعة البشرية وفيروس سارس-كوف-2 والتهاب الكبد سي، أنه إذا تمكن من فهم الآلية الدقيقة لسبب عدم استقرار بروتين F قبل الاندماج، وخاصة لماذا من السهل فتحه، فيمكنه صنع شكل أكثر استقرارًا - وبالتالي لقاح أفضل.
قام تشو وفريقه البحثي أولًا بتحليل بروتينات F المستخدمة في تطوير أربعة لقاحات موجودة ضد فيروس المخلوي التنفسي - Arexvy وmResvia وAbrysvo المتوفرة تجاريًا، بالإضافة إلى لقاح تجريبي وصل إلى المرحلة الثالثة من التجارب.
وقد اكتشف الباحثون أن بعض بروتينات F التي تسبق الاندماج تبدو غير مستقرة، وتتحول في بعض الأحيان إلى شكل مفتوح، أو حتى إلى شكل أقل استحسانا، وهو شكل ما بعد الاندماج.
وكشف تحليل هيكلي مفصل عن وجود "بقعة حمضية" تقع في وسط بنية ما قبل الاندماج مع ثلاث جزيئات مشحونة إيجابيا تتنافر مع بعضها البعض، وهي جاهزة لدفع بروتين RSV F إلى الانفتاح عند أدنى اضطراب، مثل المحول المحمل بنابض.
يقول تشو: "إن هذه سمة مذهلة يكتسبها الفيروس أثناء التطور للتحكم في حركة البروتين الرئيسي الخاص به، ولحسن الحظ، يمكننا التغلب على هذه السمة أيضًا، إما بالقوة الغاشمة أو، وهو الأفضل، من خلال طفرة ذكية تعالج بشكل مباشر مصدر المشكلة، البقعة الحمضية".
قام تشو بإعادة هندسة بروتين RSV F من خلال تغيير زوج من الجزيئات في مركزه، مما أدى إلى تحويل قوة الطرد الخارجية إلى قوة جذب. ثم أظهر فريقه أن هذا البروتين الجديد F كان أكثر استقرارًا في المختبر وعمل بنجاح على تطعيم الفئران ضد RSV.
يقول تشو: "يشير هذا إلى أننا قد نكون قادرين على اتباع نهج مماثل مع بروتينات F الفيروسية الأخرى، وعلى أقل تقدير، يمكننا البحث عن بقع مماثلة مثيرة للاشمئزاز في بنيتها أثناء تصميم اللقاحات".
في بروتين hMPV F، لم يجد تشو نفس الرقعة من الجزيئات الطاردة - بدلًا من ذلك، استخدم رابطة كيميائية قوية كمحلول "قوة غاشمة" لربط البروتين معًا. ومرة أخرى، كان البروتين المعدل مستقرًا بما يكفي ليظل سليمًا كلقاح.
وفي دراسات مستقبلية، يخطط تشو لتطوير لقاح تجريبي باستخدام منصة جزيئات بروتينية ذاتية التجميع (SApNP) التي وردت في عمله الأخير لتوصيل بروتينات RSV وhMPV F إلى جسم الإنسان.
يقول تشو: "سيكون هذا هو لقاحنا المركب من الجيل التالي لفيروس RSV/hMPV".